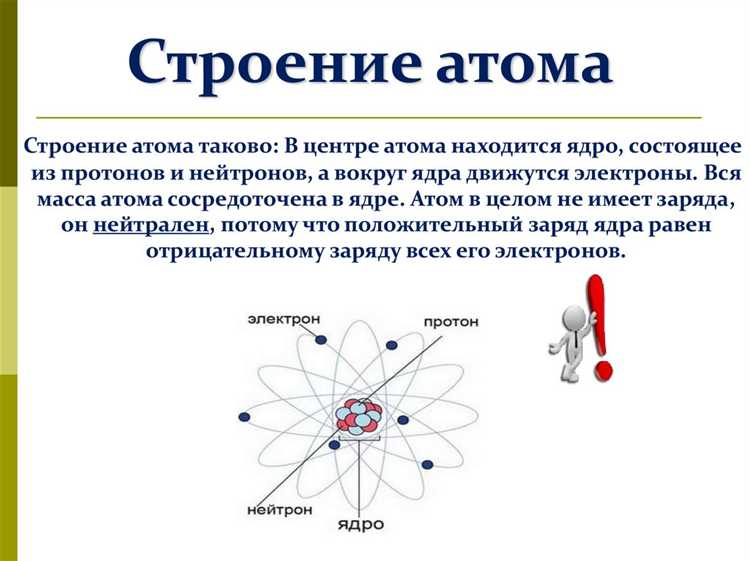
Энергия, испускаемая атомом при переходе электрона между энергетическими уровнями, выделяется в виде кванта света – фотона. Такая порция энергии называется квант. Она определяется дискретностью энергетических уровней и соответствует разнице между начальными и конечными состояниями электрона.
Величина энергии кванта связана с частотой излучения через соотношение E = hν, где h – постоянная Планка, равная примерно 6,626·10⁻³⁴ Дж·с, а ν – частота излучения в герцах. Эта формула лежит в основе квантовой теории и позволяет точно рассчитывать энергию фотонов, испускаемых атомом.
Понимание природы и величины квантов важно для таких приложений, как спектроскопия, лазерные технологии и квантовая электроника. Например, спектральные линии в оптических спектрах элементов определяются именно частотами этих квантов энергии, что обеспечивает метод идентификации и анализа атомных структур.
Происхождение и природа квантов энергии в атомном излучении
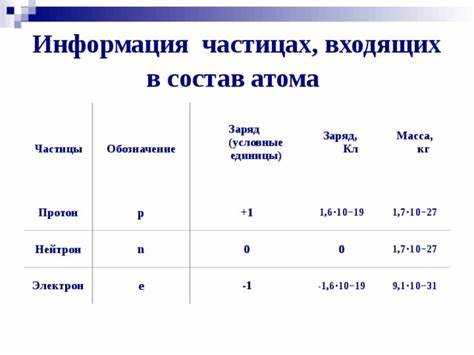
Кванты энергии, испускаемые атомом, возникают вследствие переходов электронов между дискретными энергетическими уровнями. Эти уровни формируются в результате решения уравнения Шредингера для атома с учетом электростатического взаимодействия между электроном и ядром.
Основные положения, определяющие природу квантов энергии:
- Энергетические состояния электрона в атоме дискретны и характеризуются квантовыми числами.
- Переход электрона с более высокого уровня на более низкий сопровождается испусканием фотона с энергией, равной разности уровней: E = hν, где h – постоянная Планка, ν – частота излучения.
- Энергия квантов фиксирована и не принимает произвольных значений, что отражает фундаментальную дискретность энергетических процессов в микромире.
Процессы, влияющие на формирование и свойства квантов энергии:
- Квантование энергии: возникает из условий стационарности волновой функции электрона и ограниченности разрешенных решений уравнения Шредингера.
- Спин-орбитальное взаимодействие: вызывает расщепление уровней, что приводит к появлению множества близких энергетических состояний и разнообразию излучаемых квантов.
- Влияние внешних полей: магнитные и электрические поля изменяют спектр излучения, что объясняется эффектами Зеемана и Штарка.
Рекомендации для анализа и использования квантов энергии атомного излучения:
- Для точного определения энергии квантов следует применять спектроскопию с высоким разрешением, позволяющую выявлять мелкие спектральные линии.
- Моделирование переходов лучше строить на основе многотелевых квантово-механических методов, учитывающих корреляции электронов.
- Использование лазерных методов возбуждения позволяет управлять конкретными переходами и, соответственно, энергией излучаемых квантов.
Связь между фотоном и порцией энергии атомного излучения

Порция энергии, излучаемая атомом, напрямую связана с понятием фотона – квантового носителя электромагнитного излучения. Энергия каждого фотона определяется формулой E = hν, где h – постоянная Планка (6,626·10−34 Дж·с), а ν – частота излучения, зависящая от разницы энергетических уровней атома.
При переходе электрона с более высокого энергетического уровня на более низкий высвобождается фотон, энергия которого равна разности этих уровней. Такой переход и соответствующее излучение фиксируются как дискретные порции энергии, что объясняет квантовый характер излучения.
Экспериментально измеряемые спектры атомов состоят из отдельных линий, каждая из которых соответствует конкретной энергии фотона. Понимание этого механизма позволяет прогнозировать спектральные характеристики и точно рассчитывать энергию порций излучения, что важно для спектроскопии и квантовой оптики.
Для практических расчетов рекомендуется использовать выражение λ = c/ν, где λ – длина волны, а c – скорость света. Зная длину волны, можно определить энергию фотона и, следовательно, энергию порции атомного излучения.
Влияние квантовых переходов на величину излучаемой энергии

Энергия, излучаемая атомом при квантовом переходе, определяется разницей энергетических уровней, между которыми происходит переход. Формула для вычисления энергии фотона E = hν, где h – постоянная Планка, ν – частота излучения, напрямую связана с ΔE = E_верхнего уровня − E_нижнего уровня. Чем больше разница между уровнями, тем выше энергия и частота излучаемого фотона.
Квантовые переходы в атомах не всегда случаются между соседними уровнями. Переходы с большим ΔE создают фотон с большей энергией и более короткой длиной волны. Например, в водороде переход с третьего на первый уровень соответствует ультрафиолетовому излучению, тогда как переход со второго на первый – видимому свету красного цвета.
Величина энергии излучения ограничена конкретной структурой электронных оболочек атома и правилом отбора, регулирующим возможные переходы. Невыполнение правил отбора приводит к запрещённым или маловероятным переходам, что снижает интенсивность излучения с данной энергией.
При анализе спектров излучения важно учитывать влияние внешних факторов, таких как электромагнитное поле и температура, которые могут смещать энергетические уровни и изменять вероятность переходов. Это приводит к изменению энергии фотонов и ширине спектральных линий.
Практическое применение данных о квантовых переходах включает спектроскопию для определения состава вещества и управление лазерными системами, где строго контролируются переходы для получения необходимой длины волны и мощности излучения.
Методы измерения порции энергии, излучаемой атомом

Измерение порции энергии, излучаемой атомом, основывается на регистрации квантов света с точно известной энергией. Основной метод – спектроскопия с высокой разрешающей способностью. При этом фиксируются длины волн или частоты фотонов, что позволяет вычислить энергию излучения по формуле E = hν, где h – постоянная Планка, ν – частота.
Для точного определения энергии применяют методы лазерной спектроскопии, включая доплеровское охлаждение и задержку атомов в магнитных или оптических ловушках, что минимизирует влияние теплового расширения линий спектра. Такая техника обеспечивает разрешение до 10-6 эВ.
Дополнительно используется метод фотонной корреляционной спектроскопии для оценки временных характеристик излучения и исключения влияния фонового шума. Важен выбор калибровочных стандартов с эталонными переходами, например, линии ртути или натрия, для повышения точности измерений.
При анализе отдельных квантов энергии часто применяют сцинтилляционные детекторы и фотомножители с высоким квантовым выходом. Они регистрируют количество и энергию фотонов с чувствительностью до единиц электрона-вольт.
Рекомендуется использовать комбинацию спектроскопии с лазерным охлаждением и фотонной корреляционной техникой для комплексной оценки энергии порции, что минимизирует систематические ошибки и повышает надежность результатов.
Роль порций энергии в спектроскопии атомных линий

Порции энергии, или кванты, непосредственно связаны с переходами электронов между энергетическими уровнями атома. Каждый энергетический скачок сопровождается излучением или поглощением фотона с энергией, равной разности уровней. Именно эта дискретность энергетических порций обеспечивает появление характерных спектральных линий.
Для спектроскопии ключевым параметром является энергия кванта, вычисляемая по формуле E = hν, где h – постоянная Планка, а ν – частота излучения. Точное измерение частот позволяет идентифицировать элемент и определить состояние атома. Погрешности в определении энергии приводят к ошибкам в интерпретации спектров и затрудняют качественный анализ.
Практическое применение требует учета дополнительных факторов: доплеровского сдвига, влияния внешних полей (Зеемановское и Штарковское эффекты), а также взаимодействия между атомами. Они модифицируют энергетические уровни и, следовательно, изменяют энергию порций. Корректная интерпретация спектров невозможна без учета этих явлений.
Для повышения точности спектроскопических измерений рекомендуют использовать лазерную спектроскопию с узкополосными источниками и методики квантовой оптики, позволяющие изолировать отдельные переходы и точно определить энергию порций. В расчетах часто применяют современные методы численного моделирования с учетом квантовой механики и электродинамики.
Применение знаний о порциях энергии в современной физике и технологиях

Понимание дискретных порций энергии, испускаемых атомами, лежит в основе спектроскопии – ключевого метода анализа химического состава и физических свойств веществ. Спектральные линии, соответствующие квантам энергии, позволяют определять элементный состав далеких звезд и планет с высокой точностью.
В квантовой оптике управление отдельными энергетическими переходами атомов применяется для создания лазеров с заданной длиной волны. Это обеспечивает высокую когерентность и мощность излучения, необходимую в медицине, телекоммуникациях и производстве микроэлектроники.
Знания о порциях энергии используются при разработке квантовых вычислительных устройств, где атомные переходы служат основой для реализации кубитов. Контроль энергии возбуждения позволяет повышать стабильность и точность квантовых операций.
В нанотехнологиях измерение и манипуляция энергетическими уровнями атомов и молекул помогают создавать материалы с уникальными оптическими и электронными свойствами, например, для сенсоров и фотонных устройств.
Рекомендовано интегрировать спектроскопические методы в процессы контроля качества материалов, а также использовать лазерные технологии, основанные на квантовании энергии, для улучшения точности обработки и диагностики в промышленности.
Вопрос-ответ:
Как называется единица измерения энергии, которую излучает атом?
Энергия, излучаемая атомом при переходе между энергетическими уровнями, обычно измеряется в электронвольтах (эВ). Это удобная единица для описания квантовых процессов на атомном уровне, поскольку 1 эВ соответствует энергии, которую приобретает электрон при прохождении через разность потенциалов в 1 вольт.
Почему энергия, излучаемая атомом, связана с конкретными квантовыми уровнями?
Атомы имеют дискретные энергетические уровни, которые определяются состояниями электронов в них. При переходе электрона с одного уровня на другой атом излучает или поглощает энергию строго определённого размера. Это связано с квантовыми законами, которые ограничивают возможные значения энергии, поэтому излучение происходит порциями, соответствующими разнице между уровнями.
Можно ли измерить энергию, излучаемую атомом, напрямую? Если да, то как?
Непосредственно измерить энергию излучаемого атомом фотона сложно, но это возможно с помощью спектроскопии. Спектр излучения показывает линии, каждая из которых соответствует фотону с определённой энергией. Измеряя длину волны или частоту излучения, можно вычислить энергию по формуле Эйнштейна — E = hν, где h — постоянная Планка, а ν — частота света.
Что влияет на величину энергии, которую излучает атом при переходе электрона между уровнями?
Основным фактором является разница энергий между двумя электронными уровнями в атоме. Чем больше эта разница, тем более энергичный фотон излучается. Эта разница зависит от структуры атома и распределения электронов, которые определяются типом атома и его химическим состоянием.
Почему излучаемая атомом энергия не бывает произвольной величины, а только определённой порцией?
Причина в квантовой природе атома. Электроны могут занимать только дискретные уровни энергии, а не любое значение. Поэтому переход происходит между конкретными уровнями, и энергия излучаемого фотона равна разнице между этими уровнями. Это фундаментальный принцип квантовой механики, который объясняет квантование энергии в атомах.
Как называется единица измерения количества энергии, которую испускает атом при переходе между энергетическими уровнями?
Количество энергии, излучаемой атомом при переходе электрона с одного энергетического уровня на другой, обычно выражается в виде квантов энергии — фотонов. Энергия этих фотонов измеряется в джоулях или электронвольтах, при этом конкретная величина энергии зависит от разницы между начальными и конечными уровнями. Часто в спектроскопии и атомной физике для описания такой энергии используется понятие «квант энергии» или просто «фотон». Это название отражает дискретный характер излучаемой энергии.