
В 1911 году Эрнест Резерфорд опубликовал результаты эксперимента по рассеянию альфа-частиц, проведённого совместно с Гейгером и Марсденом. Этот опыт, в котором альфа-частицы направлялись на тонкую золотую фольгу, привёл к революционному пересмотру представлений о структуре атома. Ожидалось, что все частицы пройдут сквозь фольгу с незначительным отклонением, однако некоторые из них отражались под большими углами, что опровергало модель Томсона.
Ключевое заключение Резерфорда состояло в том, что почти вся масса атома сосредоточена в его центральной области – ядре, обладающем положительным зарядом. Электроны, согласно новой модели, обращаются вокруг ядра, напоминая планеты на орбитах. Эта ядерная модель атома впервые ввела представление о внутреннем устройстве вещества, в котором объём атома в основном занят пустым пространством.
Практическая значимость открытия заключалась в создании базы для развития квантовой физики и ядерной энергетики. Без чёткого понимания пространственного распределения зарядов и масс внутри атома было невозможно объяснить ни стабильность атомов, ни характер спектров излучения. Именно модель Резерфорда сделала возможным дальнейшее развитие атомных теорий и заложила фундамент для модели Бора и всей последующей атомной физики.
Как был поставлен опыт с золотой фольгой и почему он стал решающим

В 1909 году Эрнест Резерфорд совместно с Гансом Гейгером и Эрнестом Марсденом провёл эксперимент, целью которого было изучение распределения заряда в атоме. Для этого использовалась чрезвычайно тонкая золотая фольга – всего несколько сотен атомов в толщину. В качестве источника альфа-частиц применялся радиоактивный изотоп радия, помещённый в свинцовый блок с узким отверстием, создающим направленный пучок частиц.
Фольгу облучали этим пучком, а вокруг неё располагался экран, покрытый сульфидом цинка, вспыхивающий при попадании альфа-частиц. Наблюдения проводились в темноте с помощью микроскопа, что позволяло фиксировать отдельные вспышки. Ожидалось, что альфа-частицы будут проходить через фольгу без значительного отклонения, как предсказывала модель атома Томсона.
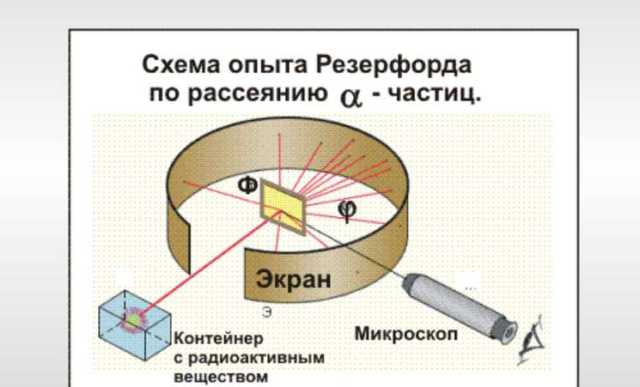
Опыт с золотой фольгой стал решающим, поскольку впервые предоставил экспериментальное подтверждение существования ядра и положительного заряда, сосредоточенного в его пределах. Это стало фундаментом современной ядерной физики и изменило представление о строении материи.
Что наблюдали ученики Резерфорда при рассеянии альфа-частиц

В 1909 году под руководством Эрнеста Резерфорда, физики Ганс Гейгер и Эрнест Марсден провели серию экспериментов, направленных на исследование поведения альфа-частиц при прохождении через тонкий золотой лист. Ученые использовали источник альфа-излучения (радиоактивный полоний), узкий пучок которого направлялся на золотую фольгу толщиной менее одного микрометра. Детектор, покрытый сульфидом цинка, позволял фиксировать вспышки при попадании альфа-частиц.
Ожидалось, что альфа-частицы пройдут сквозь фольгу с минимальными отклонениями, исходя из модели Томсона. Однако наблюдения показали следующее:
- Большинство частиц действительно проходили через фольгу практически без изменения направления, что соответствовало предположениям о малой плотности атома.
- Незначительная часть альфа-частиц отклонялась на углы до 10°, что указывало на наличие в атоме некоторого центра с высокой массой и положительным зарядом.
- Крайне редкие частицы отражались почти назад – на углы более 90°. Это стало критическим наблюдением: подобное поведение невозможно в рамках модели атома с равномерно распределённым зарядом.
Какие расчёты позволили Резерфорду предположить наличие ядра

Альфа-эксперимент, проведённый в 1909 году Гейгером и Марсденом под руководством Резерфорда, дал количественные данные, не совместимые с моделью атома Томсона. Ключевые расчёты начались с анализа углов отклонения альфа-частиц при прохождении через тонкую золотую фольгу.
- Резерфорд исходил из закона кулоновского взаимодействия: потенциальная энергия взаимодействия α-частицы (заряд +2e) и точечного заряда (предположительно ядра атома) определялась выражением U = (1/4πε₀) × (2eZe)/r, где Z – заряд ядра, r – расстояние сближения.
- Максимальный угол отклонения рассчитывался на основе закона сохранения энергии и импульса. При сближении α-частицы на минимальное расстояние её кинетическая энергия переходила в потенциальную. Это позволило вычислить минимальное расстояние до ядра:
r_min = (1/4πε₀) × (2eZe) / (½mv²)
- При энергиях α-частиц порядка 5 МэВ и наблюдаемых отклонениях свыше 90°, расчёт давал r_min ≈ 10⁻¹⁴ м – в тысячи раз меньше размеров атома (~10⁻¹⁰ м). Это указывало на сосредоточение положительного заряда и массы в крайне малом объёме.
- Статистика отклонений, собранная на десятках тысяч α-частиц, показала, что доля частиц с большими углами отклонения (более 90°) согласуется с моделью точечного положительного центра, а не с равномерно распределённым зарядом.
Сравнение теоретического распределения углов отклонения по формуле Резерфорда:
dN/dθ ∝ 1/sin⁴(θ/2)
- Подтвердило гипотезу о существовании центра с высокой плотностью заряда.
- Различие между экспериментальными данными и моделью «пудинга» Томсона стало математически очевидным: отклонения при центральных столкновениях были невозможны без сосредоточенного ядра.
Чем модель Резерфорда отличается от модели Томсона

Модель Томсона (1897) представляла атом в виде положительно заряженной сферы, внутри которой равномерно распределены отрицательные электроны. Эта концепция, получившая название «пудинговой модели», не предусматривала наличие ядра и предполагала равномерное распределение массы и заряда.
Модель Резерфорда (1911) была основана на результатах эксперимента по рассеянию альфа-частиц. Наблюдение резких отклонений части заряженных частиц от их траектории указывало на наличие массивного положительного центра – ядра. Согласно Резерфорду, электроны вращаются вокруг ядра по орбитам, а основная масса атома сосредоточена в его центре.
Ключевое отличие заключается в структуре: у Томсона отсутствует центр масс и зарядов, у Резерфорда – компактное положительное ядро с почти пустым пространством вокруг, где движутся электроны. Модель Томсона не объясняет отклонения альфа-частиц, а модель Резерфорда делает это с высокой точностью.
С теоретической точки зрения, модель Резерфорда закладывает основу для планетарной концепции атома, опровергая идею о сплошной структуре, предложенной Томсоном. Это стало отправной точкой для дальнейших квантовых исследований, включая модель Бора.
Ключевое открытие заключалось в том, что почти все масса атома сосредоточена в ядре, занимающем ничтожно малый объём по сравнению с атомом в целом. Это объяснило резкое отклонение альфа-частиц от первоначальной траектории, что было невозможно в рамках модели Томсона.
Последствия этого открытия носили не теоретический, а прикладной характер. Появилась возможность изучать свойства ядер – их заряд, массу, изотопный состав. Начались эксперименты по ядерным реакциям, включая искусственную трансмутацию элементов, впервые реализованную самим Резерфордом в 1919 году при бомбардировке азота альфа-частицами.
Без модели атома с ядром невозможно было бы сформулировать правила ядерных взаимодействий и уравнения сохранения, такие как сохранение числа нуклонов и электрического заряда. Всё это составляет фундамент современной ядерной физики и энергетики.
Какие ограничения имеет планетарная модель атома

Планетарная модель атома, предложенная Резерфордом, имела ряд существенных ограничений, выявленных в ходе дальнейших исследований:
- Стабильность орбит электрона не объясняется – согласно классической электродинамике, ускоренно движущийся электрон должен излучать энергию и падать на ядро, что не наблюдается на практике.
- Отсутствие объяснения дискретности спектров – модель не предсказывает квантованные энергетические уровни, необходимые для интерпретации наблюдаемых линий излучения и поглощения.
- Не учитывает волновую природу электрона, что позднее показала теория де Бройля и квантовая механика.
- Не описывает влияние спина электрона и магнитных моментов, важных для точного понимания атомной структуры и спектроскопии.
- Неспособность применяться к более сложным атомам – модель работает лишь для водородоподобных систем, не объясняя поведение многозначных электронов и их взаимодействия.
Рекомендации для дальнейших исследований включают разработку моделей, основанных на квантовых принципах и учитывающих корпускулярно-волновой дуализм, что и было реализовано в последующих теориях Бора и квантовой механике.
Как эксперимент Резерфорда применяется в современной науке

Эксперимент Резерфорда с рассеянием альфа-частиц на тонкой золотой фольге заложил основы понимания атомной структуры и остаётся ключевым в современных исследованиях. В ядерной физике методика рассеяния продолжает использоваться для определения размеров и формы ядер различных элементов, включая нестабильные изотопы. Современные ускорители частиц применяют принципы рассеяния для изучения взаимодействий на субатомном уровне, выявляя новые свойства фундаментальных частиц.
В материаловедении аналогичные методы помогают анализировать структуру наноматериалов и тонких плёнок, выявляя дефекты и неоднородности с нанометровой точностью. В медицине, в частности в радиотерапии и диагностике, принципы, выведенные из эксперимента Резерфорда, используются для моделирования взаимодействия ионизирующего излучения с тканями, что повышает точность дозирования и эффективность лечения.
Современные методики рассеяния, основанные на идеях Резерфорда, интегрированы в спектроскопические и аналитические приборы, позволяя исследовать химический состав и структурные особенности веществ без разрушения образца. Рекомендовано использовать эти методы при разработке новых материалов и фармацевтических соединений для контроля качества и оптимизации процессов синтеза.
Вопрос-ответ:
Как Резерфорд объяснил структуру атома в своей модели?
Резерфорд предложил, что атом состоит из маленького плотного ядра с положительным зарядом, вокруг которого движутся электроны. Он пришёл к этому выводу после проведения эксперимента с рассеянием альфа-частиц, когда большинство частиц проходили сквозь тонкую металлическую фольгу, а некоторые отражались под большими углами. Это свидетельствовало о том, что внутри атома есть компактное ядро, где сосредоточена почти вся масса и заряд.
Почему эксперимент Резерфорда с альфа-частицами был важен для понимания атома?
Эксперимент позволил получить прямые доказательства существования ядра в атоме. До этого предполагалась модель, где заряд распределён равномерно по всему объёму атома. Однако отклонение альфа-частиц на большие углы показало, что положительный заряд сосредоточен в небольшой области, что опровергло предыдущие идеи и изменило представления о внутреннем строении атома.
Какие ограничения были у модели атома Резерфорда?
Хотя модель объясняла наличие ядра, она не могла объяснить стабильность атома и почему электроны не притягиваются к ядру и не падают на него. Также она не раскрывала природу движения электронов вокруг ядра и не учитывала квантовые явления, которые позже стали основой для более точных моделей.
Как открытие Резерфорда повлияло на развитие физики и химии?
Открытие ядра стало фундаментом для развития ядерной физики и квантовой механики. Оно позволило учёным лучше понять строение материи, что в дальнейшем привело к созданию новых теорий и технологий, включая ядерную энергию и современные методы анализа веществ. Кроме того, это открыло путь к более точным моделям атома и объяснению химических свойств элементов.
Что именно показал эксперимент с рассеянием альфа-частиц, проведённый Резерфордом?
Эксперимент выявил, что большинство альфа-частиц проходят через тонкую золотую фольгу без отклонений, что указывает на то, что атом в основном пустое пространство. Однако небольшое количество частиц резко меняли направление или отражались назад, что свидетельствует о столкновении с очень плотным и маленьким объектом — ядром. Это стало ключевым доказательством наличия компактного центра с положительным зарядом в атоме.






