
Кислород (O2) имеет молекулярную массу 32 г/моль. Он состоит из двух атомов кислорода, каждый из которых весит примерно 16 г/моль. Углекислый газ (CO2) состоит из одного атома углерода (12 г/моль) и двух атомов кислорода, что в сумме дает 44 г/моль. Следовательно, углекислый газ тяжелее кислорода примерно на 37,5%.
Разница в молекулярной массе имеет практическое значение. При утечке углекислого газа он скапливается ближе к поверхности, поскольку его плотность при стандартных условиях около 1,98 кг/м³, тогда как у кислорода – примерно 1,43 кг/м³. Это важно учитывать при проектировании вентиляции в помещениях с высоким риском накопления CO2.
При анализе дыхательных смесей или создании систем жизнеобеспечения (например, в подводных лодках или космических станциях) необходимо учитывать, что вытеснение кислорода углекислым газом может произойти незаметно, особенно в плохо проветриваемых пространствах. Даже незначительное превышение допустимой концентрации CO2 может привести к физиологическим нарушениям у человека.
Что тяжелее: кислород или углекислый газ

Молярная масса кислорода (O₂) составляет 32 г/моль. Он состоит из двух атомов кислорода, каждый из которых имеет атомную массу 16 г/моль.
Углекислый газ (CO₂) имеет молярную массу 44 г/моль: один атом углерода (12 г/моль) и два атома кислорода (по 16 г/моль). Это делает CO₂ значительно тяжелее кислорода.
При прочих равных условиях углекислый газ оседает ниже в атмосфере, особенно в закрытых и плохо вентилируемых помещениях. Это критично при работе в шахтах, подвалах, танках и герметичных пространствах, где накапливание CO₂ может привести к гипоксии.
Рекомендация: в местах с возможным скоплением CO₂ устанавливай датчики концентрации углекислого газа. При показателях выше 1000 ppm – обеспечивай немедренную вентиляцию.
Сравнение молярных масс кислорода и углекислого газа

Молярная масса кислорода (O2) составляет 32 г/моль. Это значение получено путем удвоения атомной массы кислорода (16 г/моль × 2), поскольку молекула кислорода состоит из двух атомов.
Молярная масса углекислого газа (CO2) выше и составляет 44 г/моль. Это сумма атомной массы углерода (12 г/моль) и удвоенной атомной массы кислорода (16 г/моль × 2).
- O2: 32 г/моль
- CO2: 44 г/моль
Разница составляет 12 г/моль, что делает углекислый газ существенно тяжелее кислорода. Это критично при расчетах в газовой промышленности, вентиляции, хранении и транспортировке газов.
- Для замещения воздуха углекислым газом необходимо учитывать его большую плотность – он оседает ниже кислорода.
- При утечках CO2 в закрытых помещениях риск удушья возрастает быстрее, чем при утечках кислорода.
- При расчете стехиометрии горения учитывается больший вклад CO2 в массу продуктов реакции.
Как масса газа влияет на его поведение в атмосфере

Молярная масса газа определяет его распределение в атмосфере и взаимодействие с другими компонентами воздуха. Углекислый газ (CO₂) имеет молярную массу 44 г/моль, в то время как кислород (O₂) – 32 г/моль. Эта разница напрямую влияет на вертикальное и горизонтальное поведение газов.
- Более тяжёлые газы концентрируются ближе к земной поверхности при отсутствии турбулентности. CO₂, как более тяжёлый, скапливается в низинах, подвалах, шахтах.
- При температурных инверсиях тяжёлые газы хуже поднимаются, усиливая концентрацию у земли. Это особенно актуально в городах с интенсивным транспортом.
- Газы с большей массой медленнее диффундируют. Углекислый газ распространяется медленнее кислорода, что снижает его скорость проникновения в верхние слои атмосферы без внешнего воздействия.
- Масса влияет на тепловое поведение. Тяжёлые газы, как правило, обладают большей теплоёмкостью, что влияет на локальные температурные аномалии и эффект теплоизоляции у поверхности.
- При работе в закрытых помещениях с органическими материалами рекомендуется вентиляция снизу – CO₂ скапливается у пола.
- При моделировании загрязнения учитывать стратификацию: тяжёлые газы не равномерно распределяются по высоте.
- Для мониторинга утечек CO₂ датчики размещают ближе к поверхности, а не на уровне дыхания.
Итог: масса газа – ключевой параметр при оценке его поведения в атмосфере, особенно в прикладных задачах вентиляции, охраны труда и моделирования климатических процессов.
Почему углекислый газ оседает в низинах
Молярная масса углекислого газа (CO₂) составляет 44 г/моль, тогда как у кислорода (O₂) – 32 г/моль. Из-за большей плотности CO₂ тяжелее воздуха и стремится к накоплению в пониженных участках рельефа.
При отсутствии сильной турбулентности или ветра, особенно ночью или в утренние часы, CO₂ не рассеивается, а накапливается в замкнутых или плохо проветриваемых низинах, таких как овраги, котлованы, подвалы. Это связано с тем, что плотный углекислый газ вытесняет более лёгкие газы вверх, образуя опасную для дыхания зону.
На склонах вулканов, например, CO₂, выделяющийся из трещин, может достигать смертельно высоких концентраций в углублениях. Аналогичная ситуация наблюдается в винодельческих подвалах, где ферментация сопровождается активным выделением CO₂.
Чтобы избежать скопления углекислого газа, необходимо обеспечить эффективную вентиляцию низинных участков. На производствах и в замкнутых пространствах используют датчики концентрации CO₂ и системы принудительной вытяжки. Рекомендуется регулярно проводить замеры, особенно в утренние часы, когда концентрация может быть максимальной.
Как температура влияет на плотность кислорода и CO₂
Плотность газов напрямую зависит от температуры по закону Бойля – Мариотта и уравнению состояния идеального газа. При повышении температуры молекулы приобретают большую кинетическую энергию, увеличивая объем и уменьшая плотность.
При температуре 0 °C и нормальном давлении плотность кислорода составляет около 1,429 кг/м³, а углекислого газа – 1,977 кг/м³. При нагревании до 20 °C плотность кислорода уменьшается до ~1,331 кг/м³, CO₂ – до ~1,842 кг/м³. Таким образом, углекислый газ остается плотнее кислорода на всём температурном диапазоне, но абсолютное значение разницы снижается.
Понижение температуры увеличивает плотность. При −50 °C плотность кислорода возрастает до ~1,692 кг/м³, CO₂ – до ~2,255 кг/м³. Это критично для расчётов в криогенной технике и при моделировании атмосферы на больших высотах, где плотности сильно варьируются с температурой.
Для инженерных расчетов рекомендуется использовать уравнение состояния: ρ = (P·M)/(R·T), где ρ – плотность, P – давление, M – молярная масса, R – универсальная газовая постоянная, T – температура в кельвинах. Учитывая, что молярная масса CO₂ (44 г/моль) почти в два раза выше, чем у O₂ (32 г/моль), даже при одинаковых условиях CO₂ всегда будет плотнее.
При температурных колебаниях в закрытых объемах необходимо учитывать изменение плотности для корректной вентиляции, хранения и транспортировки газов. В баллонах и системах подачи ошибки в расчётах могут привести к недостаточной или избыточной подаче газа.
Применение газов с разной плотностью в промышленности
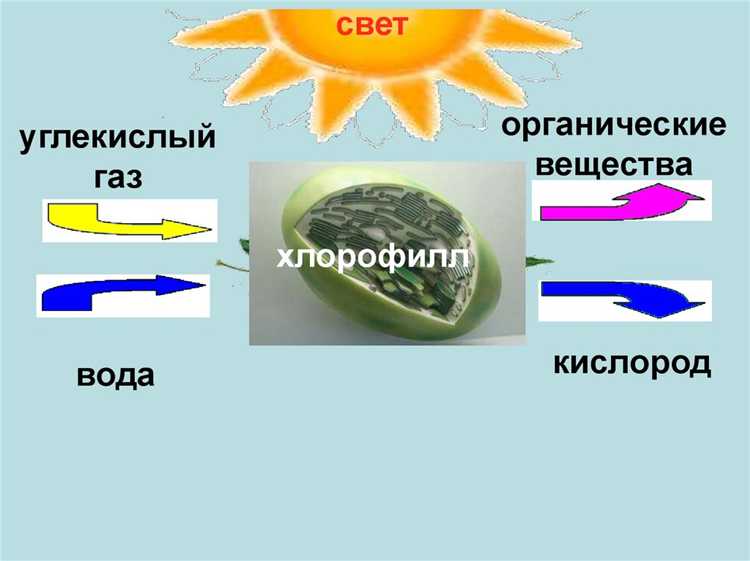
Плотность газов напрямую влияет на их использование в технологических процессах. Кислород с молекулярной массой 32 г/моль и плотностью около 1,43 кг/м³ при нормальных условиях применяется для интенсивного окисления в металлургии, сварочных процессах и химическом синтезе. Его сравнительно низкая плотность обеспечивает эффективное перемешивание и доставку в зоны реакции.
Углекислый газ с молекулярной массой 44 г/моль и плотностью около 1,98 кг/м³ используется как инертный газ для вытеснения кислорода и предотвращения окислительных процессов. Высокая плотность CO₂ позволяет создавать защитные слои над продуктами, например, при сварке или упаковке пищевых товаров, что снижает контакт с воздухом и продлевает срок хранения.
В системах пожаротушения плотность углекислого газа способствует его оседанию и более быстрому вытеснению кислорода, что эффективнее гасит пламя. В то же время кислород в чистом виде из-за низкой плотности менее применим в таких задачах, так как поддерживает горение.
Использование газов с разной плотностью требует точного расчёта подачи и распределения. Например, в процессах экстракции и сушки газовые потоки регулируют с учётом веса молекул для оптимального контакта с веществом. Несоблюдение этих параметров снижает эффективность и увеличивает расход сырья.
Для автоматизированных систем контроля атмосферы производств учитывают разницу в плотности при проектировании вентиляции и очистки воздуха. Газы с высокой плотностью легче локализуются в низких зонах, что требует дополнительного контроля для безопасности персонала и предотвращения концентраций вредных веществ.
Таким образом, выбор газа с учётом плотности позволяет повысить производительность, снизить энергозатраты и обеспечить безопасность технологических операций.
Влияние массы газов на вентиляцию и воздухообмен

Молекулярная масса газов напрямую влияет на их плотность, что определяет скорость и характер перемещения в вентиляционных системах. Кислород (O₂) имеет молекулярную массу 32 г/моль, а углекислый газ (CO₂) – 44 г/моль. Более высокая плотность CO₂ приводит к его склонности к оседанию в нижних слоях помещений при недостаточном перемешивании воздуха.
Основные последствия различий в массе газов для вентиляции:
- Углекислый газ тяжелее воздуха и может скапливаться у пола, создавая зоны с повышенной концентрацией, если отсутствует эффективный воздухообмен на уровне пола.
- Кислород, будучи легче, распределяется равномернее и быстрее достигает верхних слоев воздуха, что важно для дыхания и предотвращения гипоксии.
- Тяжёлые газы требуют целенаправленной организации приточно-вытяжной вентиляции с размещением заборных и вытяжных решёток в нижних зонах помещения для предотвращения застойных зон.
Рекомендации для проектирования систем вентиляции с учётом массы газов:
- Использовать вентиляционные отверстия и диффузоры на разных уровнях помещения для обеспечения перемешивания воздуха и предотвращения локальных скоплений тяжелых газов.
- Обеспечивать минимальную скорость воздушного потока не менее 0,1 м/с у пола, чтобы углекислый газ не накапливался в нижних зонах.
- В помещениях с повышенной выработкой CO₂ (лаборатории, спортзалы) предусматривать отдельные вытяжные системы с забором воздуха у пола.
- Проводить регулярный мониторинг концентраций CO₂ на различных высотах, чтобы выявить зоны с низкой вентиляцией и скорректировать режимы воздухообмена.
Игнорирование массы газов приводит к снижению эффективности вентиляции, ухудшению качества воздуха и повышенному риску накопления вредных веществ. Точная настройка систем с учётом физико-химических свойств газов повышает безопасность и комфорт в помещениях.
Как определить, какой газ тяжелее, без лаборатории

Для сравнения плотности кислорода и углекислого газа в домашних условиях можно воспользоваться простым экспериментом с использованием двух прозрачных ёмкостей и зажжённой свечи.
Наполните одну ёмкость кислородом (например, надув её свежим воздухом, где содержится примерно 21% кислорода), а другую – углекислым газом. Углекислый газ можно получить, растворив пищевую соду в уксусе или используя газ из бутылки с газировкой, аккуратно направляя его в ёмкость.
Опустите в каждую ёмкость зажжённую свечу. Свеча в кислороде будет гореть ярко и стабильно, в углекислом газе пламя погаснет быстро, что косвенно подтверждает наличие газа.
Чтобы определить, какой газ тяжелее, аккуратно наклоните ёмкости или переверните их. Тяжёлый газ медленнее покидает ёмкость и при наклоне из ёмкости с углекислым газом он выльется медленнее, чем из ёмкости с кислородом. Углекислый газ имеет молекулярную массу около 44 г/моль, кислород – 32 г/моль, поэтому CO₂ тяжелее и «оседает» вниз.
Также можно провести тест с наполнением сосуда углекислым газом и выпустить его через трубочку в воду – пузырьки углекислого газа будут тяжелее воздуха и задержатся у дна сосуда дольше, чем пузырьки воздуха с кислородом.
Ошибки и мифы о тяжести кислорода и углекислого газа
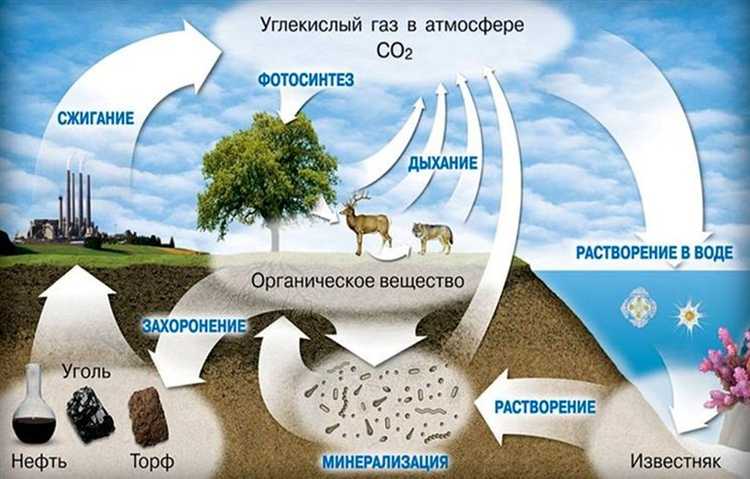
Распространено заблуждение, что кислород и углекислый газ имеют сопоставимый вес или что кислород тяжелее из-за его роли в дыхании. На самом деле, молярная масса кислорода (O₂) составляет примерно 32 г/моль, а углекислого газа (CO₂) – около 44 г/моль. Это означает, что углекислый газ примерно на 37,5% тяжелее кислорода при равных условиях.
Еще одна ошибка – считать, что углекислый газ всегда опускается вниз в атмосфере. Хотя CO₂ плотнее воздуха, в естественных условиях его распределение быстро выравнивается из-за конвекции и ветра. Только в замкнутых пространствах с плохой вентиляцией CO₂ может скапливаться у пола.
Миф о «тяжести» газов часто приводит к неправильному пониманию безопасности на производствах и в быту. Например, опасность от углекислого газа связана не столько с его весом, сколько с токсичностью и способностью вытеснять кислород в замкнутых пространствах.
Рекомендуется при работе с этими газами учитывать не только молярную массу, но и условия распространения, вентиляцию и концентрации, а не полагаться на простое сравнение веса. Точные измерения и контроль состава воздуха – ключевые меры для предотвращения инцидентов.
Вопрос-ответ:
Почему углекислый газ тяжелее кислорода?
Углекислый газ состоит из одного атома углерода и двух атомов кислорода, что придаёт ему большую молекулярную массу по сравнению с кислородом, который состоит из двух атомов кислорода. Из-за этого молекулы углекислого газа тяжелее молекул кислорода.
Как влияет разница в массе кислорода и углекислого газа на их поведение в воздухе?
Поскольку углекислый газ тяжелее кислорода, он склонен оседать ближе к поверхности земли, особенно в спокойных условиях без ветра. Кислород, будучи легче, лучше смешивается с окружающим воздухом и распределяется более равномерно.
Можно ли почувствовать разницу в тяжести воздуха, если он насыщен углекислым газом?
В обычных условиях разница в ощущении воздуха с повышенным содержанием углекислого газа не заметна для человека, так как концентрация этого газа в атмосфере обычно очень мала. Однако в замкнутых помещениях с плохой вентиляцией углекислый газ может накапливаться и создавать ощущение «тяжёлого» или «задушливого» воздуха.
Почему важно знать, что углекислый газ тяжелее кислорода в промышленности и медицине?
Знание о разнице в плотности помогает правильно организовать вентиляцию и системы удаления газов, чтобы избежать накопления углекислого газа в низких зонах помещений. В медицине это влияет на методы подачи кислорода и контроля газового состава в помещениях с пациентами.
Как измеряется масса молекул кислорода и углекислого газа и почему они отличаются?
Молекулярная масса определяется суммой атомных масс элементов в молекуле. Молекула кислорода содержит два атома кислорода с атомной массой около 16 единиц каждый, итого примерно 32. Молекула углекислого газа содержит один атом углерода (около 12) и два кислорода (2×16 = 32), всего около 44 единиц. Это и объясняет большую массу углекислого газа по сравнению с кислородом.
Почему углекислый газ тяжелее кислорода?
Молекулы углекислого газа состоят из одного атома углерода и двух атомов кислорода, что вместе даёт массу около 44 атомных единиц. В то время как молекула кислорода состоит из двух атомов кислорода с массой примерно 32 атомных единицы. Из-за большей массы одной молекулы, углекислый газ обладает большей плотностью при одинаковых условиях температуры и давления, поэтому он считается тяжелее кислорода.
Как это отличие влияет на поведение кислорода и углекислого газа в атмосфере или в помещениях?
Из-за разницы в плотности углекислый газ склонен скапливаться в нижних слоях воздуха, особенно в плохо проветриваемых помещениях или низинах на улице. Кислород, будучи легче, распределяется более равномерно в воздухе. Это может быть важно, например, для вентиляции или безопасности: углекислый газ в избытке может накапливаться у пола и создавать опасные условия для дыхания, тогда как кислород в воздухе поддерживает жизнедеятельность и обычно не оседает вниз.






