Разложение воды на водород и кислород требует экстремальных температур, превышающих 2000 °C. Этот процесс известен как термический (пиролитический) распад воды и является высокоэнергоёмким, поскольку молекулы H2O обладают прочной ковалентной связью, требующей значительного теплового воздействия для разрушения.
При температуре около 2500 °C начинает наблюдаться заметная степень диссоциации воды на H2 и O2, однако для достижения равновесного состояния с существенным выходом водорода необходимы температуры порядка 3000–3500 °C. При 3000 °C степень диссоциации составляет менее 1%, что делает данный способ малоэффективным без замкнутого цикла с быстрой сепарацией продуктов реакции.
Для лабораторных и промышленных применений прямой термический распад воды практически не используется из-за высокой энергоёмкости. Вместо этого применяются каталитические, электрохимические или термохимические методы с участием промежуточных реакций, позволяющих снизить температуру процесса до 1000–1500 °C или даже ниже при использовании многоступенчатых циклов, таких как цикл Саулье или цикл Йод-сера.
Если цель – получение водорода без выбросов CO2, предпочтительно использовать альтернативные методы, в частности, высокотемпературный паровой электролиз с температурой около 800–1000 °C, при котором эффективность выше за счёт частичной компенсации энергии теплом. Однако для чисто термического разложения следует учитывать пределы термостойкости используемых материалов, оптимизировать систему теплообмена и предусмотреть методы быстрой изоляции H2 и O2 во избежание обратной рекомбинации.
При какой температуре вода начинает термически разлагаться

Термическое разложение воды начинается при температурах свыше 2000 °C, однако значительная диссоциация молекул H2O на водород и кислород наблюдается только при температуре около 2500–3000 °C. При 3000 °C доля разложившейся воды достигает примерно 3–5% в условиях равновесия.
Процесс сильно зависит от давления: при атмосферном давлении эффективность разложения минимальна. Повышение давления до 10–20 атм позволяет увеличить степень диссоциации, но температура все равно должна превышать 2000 °C. При 4000 °C водяной пар уже диссоциирует на более чем 20%.
Технически устойчивое разложение воды термическим путем возможно только в специализированных установках с плазменными горелками или в реакторах с концентрированным солнечным излучением, где достигаются температуры свыше 2500 °C. Такие условия крайне энергозатратны, что делает метод экономически неэффективным для масштабного производства водорода без использования теплоаккумулирующих систем или катализаторов, снижающих порог температур.
Почему разложение воды требует высоких температур
- Энергия связи O–H составляет около 463 кДж/моль. Для разрыва двух таких связей в одной молекуле требуется около 926 кДж/моль.
- Температура начала термического разложения воды превышает 2000 °C. Для заметного выхода водорода необходимо достичь порядка 2500–3000 °C.
- При температуре 3000 °C степень разложения воды составляет лишь около 3–5%. Полное разложение не достигается даже при экстремальных условиях из-за сдвига равновесия обратно к образованию воды.
Основные причины высокой термической устойчивости воды:
- Малый молекулярный размер и высокая электроотрицательность кислорода приводят к прочной полярной связи.
- Стабильность молекулы поддерживается водородными связями в жидком состоянии и сильной межмолекулярной когезией.
Для повышения эффективности термического разложения применяют:
- Плазменные установки, обеспечивающие локальные температуры выше 4000 °C.
- Каталитическое воздействие в сочетании с высокотемпературной обработкой (например, с использованием оксидов металлов).
- Совмещение с термохимическими циклами (цикл Сульфур-Йод и др.), уменьшающими пиковую температуру реакции до 800–1000 °C.
Без применения подобных технологий прямой термический распад воды остается неэффективным способом получения водорода.
Роль давления в температуре разложения воды

Давление оказывает ключевое влияние на температурный порог термического разложения воды. При атмосферном давлении (1 атм) значительное разложение воды начинается при температуре около 2000°C. Однако повышение давления существенно смещает эту границу. Например, при давлении 10 атм температура, необходимая для получения сравнимого выхода водорода, увеличивается до около 2500°C, поскольку рост давления смещает равновесие реакции в сторону исходных веществ.
Согласно уравнению реакции H2O ⇌ H2 + ½O2, увеличение общего давления приводит к снижению степени диссоциации, так как реакция сопровождается увеличением количества молей газа. Это означает, что в замкнутой системе повышение давления стабилизирует воду и подавляет её разложение.
При работе с системами высокотемпературного электролиза или термохимических циклов важно учитывать, что оптимизация давления позволяет сократить энергетические потери. Для эффективного выделения водорода при минимальных затратах энергии рекомендуется использовать пониженное давление, вплоть до вакуума. При давлениях ниже 0,1 атм температура начала разложения снижается до примерно 1500–1600°C, что делает процесс менее энергоёмким.
Таким образом, контроль давления – это не просто параметр безопасности, а инструмент управления равновесием и энергоэффективностью процесса получения водорода из воды. Для промышленных установок целесообразно интегрировать системы динамического регулирования давления в зависимости от температурного режима и целевых показателей выхода водорода.
Сравнение термического и электролитического разложения воды по температурному порогу
Разложение воды на водород и кислород осуществляется двумя основными методами: термическим и электролитическим. Ключевое различие между ними – температурный режим, необходимый для протекания реакции.
- Термическое разложение начинается при температурах выше 2000 °C. Значительное разложение фиксируется при 2500–3000 °C. При 3000 °C степень диссоциации достигает около 50%. Такой температурный порог требует применения тугоплавких материалов и технологий, устойчивых к экстремальному нагреву.
- Электролиз воды возможен уже при комнатной температуре, однако эффективность процесса зависит от температуры и электролита. Наиболее распространённый диапазон – 60–90 °C, в условиях щелочного электролиза. При использовании твёрдотельных оксидных электролитов (SOEC) оптимальная температура – 700–900 °C.
Температурные особенности методов определяют их применимость:
- Термический метод экономически оправдан только при наличии источника высокотемпературного тепла, например, в ядерной энергетике или концентрированной солнечной энергетике.
- Электролиз более гибок в применении, особенно при интеграции с возобновляемыми источниками энергии. Низкий температурный порог делает его доступным в распределённых энергетических системах.
Для лабораторных и промышленных условий, где температура – критически важный параметр, электролитический метод предпочтительнее, если не предполагается использование высокотемпературных промышленных отходов или реакторов. Термический метод оправдан лишь при наличии соответствующей инфраструктуры и задач масштабного производства водорода.
Материалы, выдерживающие температуры термолиза воды

Термолиз воды начинается при температуре выше 2000 °C, однако для значительного разложения необходимы условия около 2500–3000 °C. При таких температурах выбор материалов для реакторов крайне ограничен.
Вольфрам обладает температурой плавления 3422 °C и сохраняет механическую прочность в условиях высокотемпературной диссоциации воды. Он устойчив к агрессивной среде водяного пара при условии инертной атмосферы или вакуума. Недостаток – склонность к окислению при наличии кислорода, поэтому требуется изоляция от воздуха.
Такая же устойчивость наблюдается у тантала (плавление 3017 °C), но он менее термостойкий, чем вольфрам, и дороже. Используется в специализированных вставках, где необходима коррозионная стойкость к водороду.
Углеродные материалы, включая графит, выдерживают температуры выше 3000 °C. Графит стабилен при термолизе воды, однако в кислородсодержащей среде происходит окисление. Рекомендуется применять графитовые компоненты в герметичных реакторах с контролируемой атмосферой.
Керамики на основе диоксида циркония (ZrO₂) и гафния (HfO₂) сохраняют структуру до 2700 °C и химически инертны к продуктам разложения воды. Их применяют как теплоизоляционные слои и футеровку. Однако механическая хрупкость ограничивает использование в конструктивных элементах.
Карборунд (SiC) и нитрид кремния (Si₃N₄) демонстрируют высокую термостойкость и химическую стабильность, особенно в инертной среде. SiC выдерживает до 2700 °C без разрушения, но при прямом контакте с кислородом возможна деградация поверхности.
Для стабильной работы установок термолиза воды необходимо сочетание тугоплавких металлов с защитными керамиками и инертной атмосферой. Оптимальные материалы подбираются с учетом профиля температур и наличия окислителей.
Температура разложения воды в лабораторных условиях
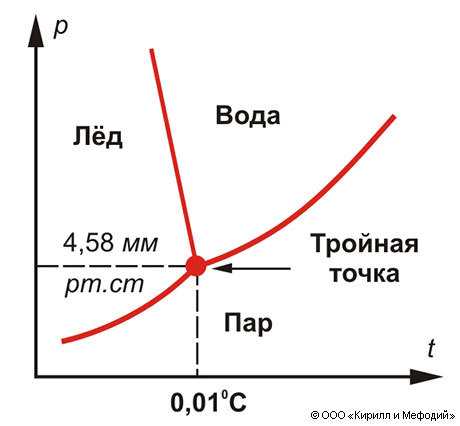
Термическое разложение воды (термолиз) в лабораторных условиях осуществляется при температурах выше 2000 °C. При такой температуре начинается значительное диссоциативное разделение молекул H2O на водород и кислород. Однако даже при 2500 °C степень разложения не превышает 3–5%, что объясняется высокой энергией связи между атомами кислорода и водорода.
Для достижения термолиза используют установки с плазменным нагревом или лазерные системы. Наиболее эффективными считаются дуговые плазмотроны, способные стабильно поддерживать температуру 3000–4000 °C. В таких условиях достигается разложение до 10% подаваемой воды, после чего требуется немедленное охлаждение продуктов реакции с целью предотвращения их рекомбинации.
Прямое нагревание воды в обычной лабораторной посуде невозможно: материалы не выдерживают необходимых температур. Используют тугоплавкие керамики или вольфрамовые элементы в вакуумной или инертной атмосфере.
Подача воды в реакционную зону производится в виде мелкодисперсного аэрозоля или пара. Контроль состава продуктов разложения осуществляется хроматографией или масс-спектрометрией. Оптимальная производительность достигается при давлении около 1 атм и температуре 3200 °C.
| Температура | Степень разложения воды | Метод нагрева |
|---|---|---|
| 2000 °C | <1% | Лазерный нагрев |
| 2500 °C | 3–5% | Плазмотрон |
| 3200 °C | 8–10% | Дуговая плазма |
При планировании эксперимента следует учитывать высокие энергетические затраты и необходимость быстрого охлаждения газов. Без этих условий термолиз воды оказывается неэффективным.
Температурные диапазоны разложения воды в промышленных процессах
Для термического разложения воды на водород и кислород в промышленных условиях требуются температуры выше 2000 °C. При таких значениях происходит диссоциация молекул воды (H2O) по уравнению: H2O ⇌ H2 + ½O2. Однако выход газов при прямом нагреве остаётся низким даже при 2500 °C, не превышая 3–5% из-за смещения равновесия.
Наиболее эффективным считается применение термохимических циклов, таких как цикл серной кислоты (IS-процесс), позволяющий осуществлять разложение воды при температуре 800–1000 °C. При этом водород отделяется в результате серии химических реакций, исключающих необходимость достижения температур полного термического распада.
Плазменные методы обеспечивают локальные температуры выше 3000 °C, при которых водяной пар быстро диссоциирует, однако высокая энергоёмкость ограничивает широкое внедрение. В индустрии такие методы применяются при необходимости получения высокочистого водорода.
Для гелиотермального разложения с использованием концентраторов солнечного излучения достигаются температуры порядка 1500–2000 °C. В сочетании с оксидными циклами (например, с участием церия или цинка) обеспечивается высокий выход водорода при сравнительно меньших энергозатратах по сравнению с прямым нагревом.
Оптимизация промышленных процессов фокусируется на снижении предельных температур до 800–1000 °C за счёт использования катализаторов и многостадийных реакционных схем, что значительно повышает общую эффективность получения водорода из воды.
Влияние примесей на температуру начала разложения воды

Чистая вода начинает термическое разложение на водород и кислород при температуре около 2000 °C. Однако наличие примесей существенно влияет на этот процесс, смещая порог начала реакции как в сторону понижения, так и повышения температуры.
Ионы щелочных металлов, таких как натрий и калий, снижают энергию активации реакции. Их присутствие в концентрациях от 0,01 до 0,1 моль/л может уменьшить температуру начала разложения на 100–200 °C за счёт катализирующего эффекта. Особенно выражен эффект при высоких температурах в плазменной среде.
Примеси переходных металлов, например ионов железа или меди, в количестве более 10⁻⁵ моль/л, ускоряют образование активных радикалов, что способствует ускоренному разложению при температуре около 1800 °C. Однако в присутствии кислородсодержащих анионов (нитратов, сульфатов) эти процессы замедляются из-за стабилизации молекул воды.
Наличие хлоридов увеличивает температуру начала разложения до 2200 °C, так как хлорид-ионы ингибируют образование свободных радикалов. Особенно выражен этот эффект при высоком давлении. Аналогично действуют фториды, которые дополнительно связываются с водородом, тормозя его высвобождение.
Для практических термолизных установок важно контролировать состав воды на уровне следовых количеств примесей. Очистка деионизацией и обратным осмосом позволяет стабилизировать температуру начала разложения в пределах ±50 °C, обеспечивая предсказуемость и эффективность процесса.
Вопрос-ответ:
При какой температуре начинается разложение воды на водород и кислород без использования катализаторов?
Чистое термическое разложение воды начинается при очень высокой температуре — примерно от 2000 °C и выше. Однако процесс становится заметно выраженным при температурах порядка 2500–3000 °C. При таких значениях вода распадается на водород и кислород в результате термической диссоциации молекул.
Почему разложение воды требует настолько высоких температур?
Молекула воды обладает прочной связью между атомами водорода и кислорода. Для её разрушения требуется значительное количество энергии. Высокая температура обеспечивает эту энергию, необходимую для преодоления потенциального энергетического барьера, чтобы инициировать диссоциацию. В обычных условиях вода очень стабильна, и её молекулы не распадаются.
Можно ли снизить температуру разложения воды при помощи катализаторов?
Да, при использовании электролиза или фотоэлектрохимических методов можно получить водород и кислород при более низких температурах. В этих случаях применяются электрическая или световая энергия и специальные катализаторы, которые позволяют разрушать молекулы воды без необходимости нагревания до нескольких тысяч градусов. Однако это уже не чисто термический, а электрохимический способ.
Какое соотношение водорода и кислорода получается при разложении воды?
При разложении одной молекулы воды (H₂O) образуется два атома водорода и один атом кислорода. В газообразной форме это выражается как соотношение 2:1 по объёму — две части водорода на одну часть кислорода. Это соотношение сохраняется независимо от метода разложения.
Какие технические трудности возникают при использовании термического разложения воды?
Основные сложности связаны с достижением и поддержанием чрезвычайно высоких температур. Это требует специальных материалов, устойчивых к нагреву, и систем, способных работать в условиях высокотемпературной агрессивной среды. Кроме того, необходимо быстро разделять образовавшиеся газы, чтобы избежать их обратного соединения в воду. Всё это делает прямое термическое разложение технологически сложным и дорогостоящим.